 English
English  日本語
日本語 
当研究室では,タッピングモード走査型プローブエレクトロスプレーイオン化法による質量分析イメージング技術と,MULTUMを用いた投影型イメージング技術およびTOF-SIMSを開発しています.
我々の体を構成する細胞では,脂質・代謝物・タンパク質などの分子量や化学的性質が異なる多彩な分子同士が相互作用し,生命活動に必要な化学反応が進むことが知られています.多彩な細胞がネットワークを作る生体組織の,疾病状態の詳細な把握や診断のためには,生体組織の複雑な化学種の分布状態を調べるイメージング技術が重要になります.試料の局所領域に含まれる成分群を抽出し,気相イオンに変換し,質量分析器に導入することで,試料内の複数の分子イオンの情報をマススペクトルとして取得することができます.個々のイオンの強度情報とその位置情報から化学成分の分布を可視化することができます.生体試料に含まれる多様な成分のイメージング技術は,バイオメディカル分野への応用が期待されています.
私たちはこれまでに,振動するキャピラリプローブ(以下,プローブ)とピコリットル液体を用いる独自の抽出イオン化法「タッピングモード走査型プローブエレクトロスプレーイオン化法(t-SPESI, tapping-mode scanning probe electrospray ionization)」を開発してきました.
Rapid Communications in Mass Spectrometry, 26 (2012), 2725-32.
Analyst, 139 (2014), 2336-41.
Journal of Mass Spectrometry, 50 (2015), 1157-1162.
Mass Spectrometry (Tokyo), 7(2) (2018), S0078.
Analytical Chemistry, 93 (2021), 2263–2272.
Analyst, 148 (2023), 1275-1284.
Analytical and Bioanalytical Chemistry, (2024)
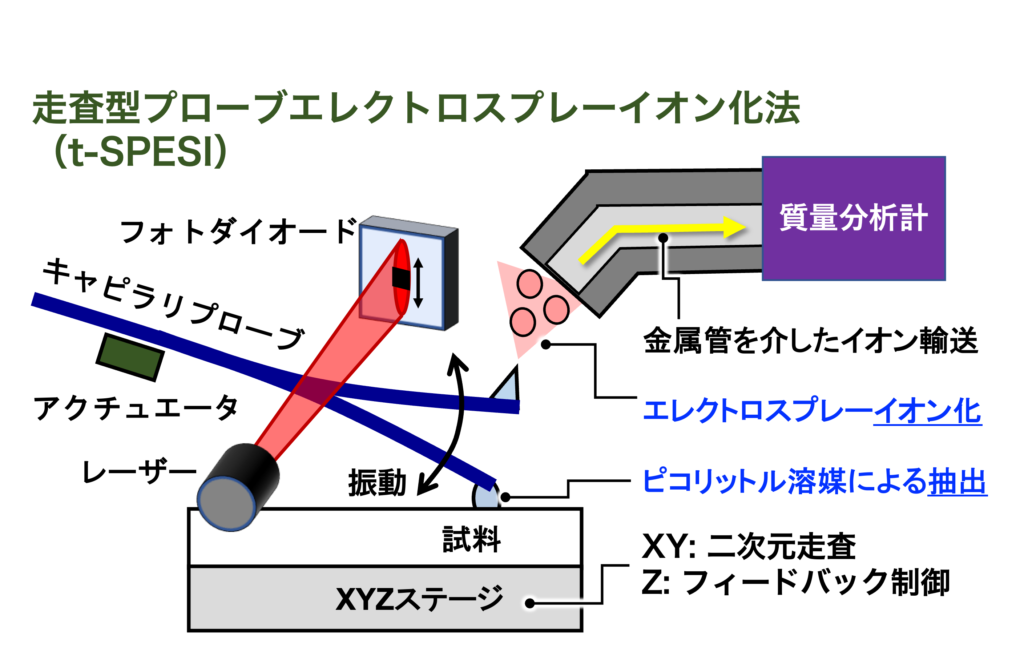
t-SPESIは,高速に振動するプローブを介して,高電圧が印加されたピコリットルの溶媒を試料に断続的に供給し,試料の局所領域に含まれる化学成分を高速に抽出・イオン化することができます.イオン化にはエレクトロスプレーイオン化法を使用し,生体分子の構造を壊さずに気相イオンに変換します.プローブを試料表面に対して二次元方向に走査することで,試料の座標情報に紐付いたマススペクトルを取得し,特定の化学成分の試料内分布を可視化することができます.
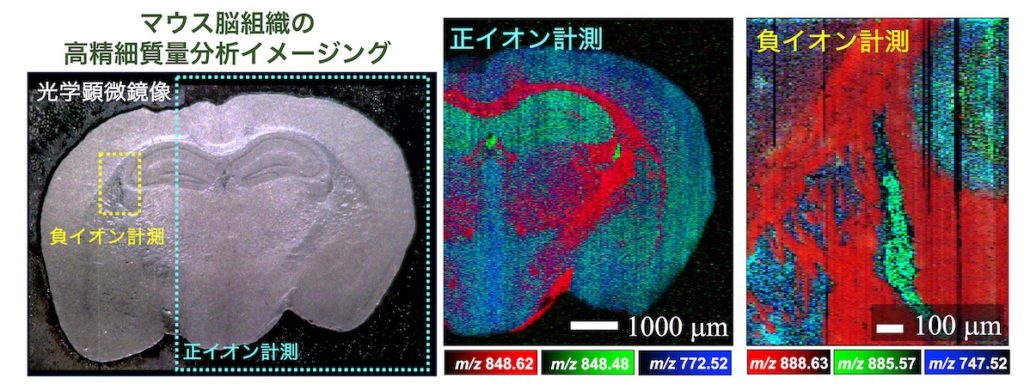
私たちは,試料の凹凸形状をナノスケールで計測することが可能な原子間力顕微鏡の要素技術をt-SPESIに融合し,試料の形状情報をリアルタイムに計測しながら抽出とイオン化を行う技術を実現しました.本技術を用いて,マウス脳組織切片の複数の脂質を空間分解能6.5マイクロメートルでイメージングでき,複数の脂質のマススペクトルパターンの違いに基づく脳内構造の分類が可能であることを示した.さらに,t-SPESIの医用応用として,ヒト疾患組織の共同研究も実施しています.大阪大学医工理連携共同研究を通じて,ヒト心臓疾患組織中の脂質成分群の多様な分布形態の可視化にも成功しました.今後は、ピコ液体の抽出イオン化過程の物理的理解と制御法の研究を進め、更なる高空間分解能イメージングを目指します。
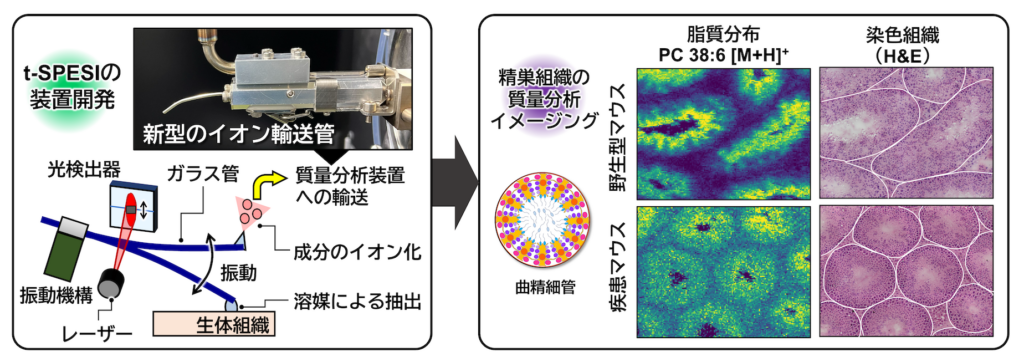
我々は、国立国際医療研究センター、実中研、株式会社島津製作所と共同で、イオンの検出感度を向上するための要素技術の開発と、疾患組織の質量分析イメージングの研究を進めてきました。マウスの精巣組織の分析を行った結果、精子が形作られる過程において特定の脂質が特徴的な分布を示し、精子形成の段階や疾患状態に依存して、それらの分布が変化することを見いだしました。精子形成の異常化など、疾患に関与する脂質の研究に、本技術は新たな知見を提供することが期待されます。
世界でも珍しい投影型イメージング質量分析計を開発しています(Review of Scientific Instruments, 92 (2021), 053706.).投影型では,サンプル表面の広い範囲を同時にイオン化して,その像を検出面に投影するとともに,質量分析も行います.現在は生命機能研究科の上田研究室と一細胞のイメージング技術の開発を行っています.
試料中に存在する原子・分子の存在量やそれらの同位体組成を、1μm以下の空間分解能で観測するため、集束イオンビームによって叩き出した試料を、高出力レーザーでポストイオン化する、2次中性粒子質量分析装置の開発を行なっています(JPS Conf. Proc., 31 (2020), 011065.).
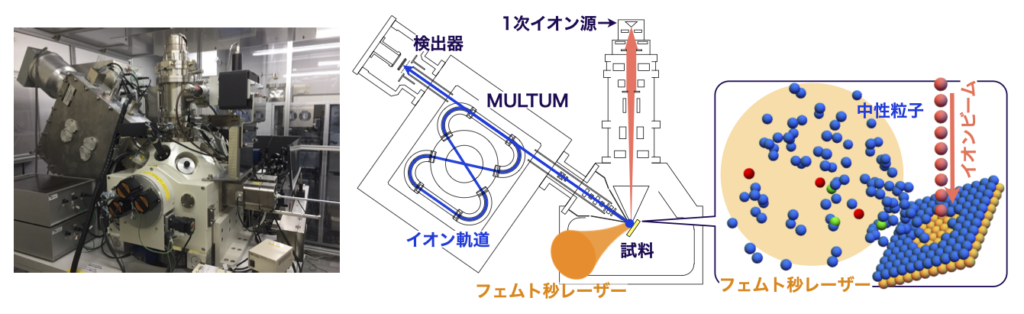
宇宙地球科学専攻寺田研究室との共同研究です.装置は寺田研に設置されています.